Autora: Maitane Expósito Corrales
La estimulación magnética transcraneal, o TMS, ayuda a muchas personas con depresión, pero no lo hace con la misma intensidad ni a la misma velocidad en todo el mundo. Eso no significa que sea una técnica “caprichosa”. Significa que actúa sobre un cerebro real, con una historia clínica concreta, mediante un protocolo técnico específico y dentro de un centro con más o menos experiencia y seguimiento. La mejor lectura de la evidencia actual no es “la TMS a veces acierta y a veces no”, sino “la TMS funciona mejor cuando se ajusta bien al paciente y se administra bien.
En depresión mayor y depresión resistente, la evidencia global es sólida. En una metaanálisis de ensayos doble ciego controlados con sham, la rTMS activa alcanzó una tasa de respuesta del 39,7% frente al 13,7% con sham, y una tasa de remisión del 35,7% frente al 8,4%, con riesgos relativos de 2,25 para respuesta y 2,78 para remisión. En guías clínicas y en práctica real, los resultados habituales se mueven aproximadamente entre un 40–50% de respuesta, con registros amplios que rondan el 60% de respuesta y el 30% de remisión, aunque estas cifras cambian según el tipo de paciente, el protocolo y el contexto en el que se trata.
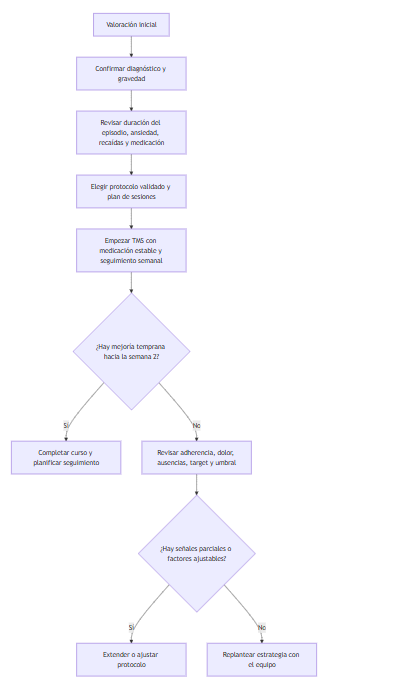
Lo importante para un paciente informado es esto: que una persona no responda igual que otra no implica que haya “fallado” ni que la técnica no valga; implica que conviene revisar bien qué diagnóstico hay, cuánto dura el episodio, qué medicación acompaña, qué protocolo se está usando, cuántas sesiones se van a completar y cómo monitoriza el equipo la evolución.